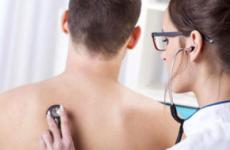
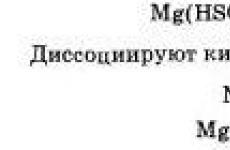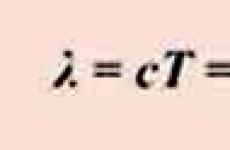10 солей химия. Соли
>> Химия: Соли, их классификация и свойства
Из всех химических соединений соли являются наиболее многочисленным классом веществ. Это твердые вещества, они отличаются друг от друга по цвету и растворимости в воде.
Соли - это класс химических соединений, состоящих из ионов металла и ионов кислотного остатка.
В начале XIX в. шведский химик И. Верцелиус сформулировал определение солей как продуктов реакций кислот с основаниями, или соединений, полученных заменой атомов водорода в кислоте металлом . По этому признаку различают соли средние, кислые и основные.
Средние, или нормальные,
- это продукты полного замещения атомов водорода в кислоте на металл.
Именно с этими солями вы уже знакомы и знаете их номенклатуру. Например:
Na2С03 - карбонат натрия, СuSO4 - сульфат меди (II) и т. д.
Диссоциируют такие соли на катионы металла и анионы кислотного остатка:
Кислые соли - это продукты неполного замещения атомов водорода в кислоте на металл.
К кислым солям относят, например, питьевую соду, которая состоит из катиона металла и кислотного однозарядного остатка НСО3. Для кислой кальциевой соли формула записывается так: Са(НСО3)2.
Названия этих солей складываются из названий солей с прибавлением слова гидро, например:

Основные соли - это продукты неполного замещения гидроксогрупп в основании на кислотный остаток.
Например, к таким солям относится знаменитый малахит (СиОН)2 С03, о котором вы читали в сказах И. Бажова. Он состоит нз двух основных катионов СиОН и двухзарядного аниона кислотного остатка СО 2- 3.
Катион СuОН+ имеет заряд +1, поэтому в молекуле два таких катиона и один двухзарядный анион СО объединены в электронейтральную соль.
Названия таких солей будут такими же, как и у нормальных солей, но с прибавлением слова гидроксо-, например (СuОН)2 СО3 - гидроксокарбонат меди (II) или АlOНСl2 - гидроксохлорид алюминия. Подавляющее большинство основных солей нерастворимы или малорастворимы. Последние диссоциируют так:
Типичные реакции солей

4. Coль + металл -> другая соль + другой металл.
Первые две реакции обмена уже были подробно рассмотрены ранее.
Третья реакция также является реакцией обмена. Она протекает между растворами солей и сопровождается образованием оселка, например:

Четвертая реакция солей связана с именем крупнейшего русского химика Н.Н.Бекетова, который в 1865 г. изучал способность металлов вытеснять из растворов солей другие металлы. Например, медь tu растворов ее солей можно вытеснять такими металлами, как магний, алюминий Al, цинк и другими металлами. А вот ртутью, серебром Аg, золотом Аu медь не вытесняется, так как атм металлы в ряду напряжений расположены правее, чем медь. Зато медь вытесняет их из растворов солей:
H. Бекетов, действуя газообразным водородом под давлением на растворы солей ртути и серебра, установил, что при атом водород, так же как и некоторые другие металлы, вытесняет ртуть и серебро из их солей.
Располагая металлы, я также водород по их способности вытеснять друг друга ял растворов солей. Бекетов составил ряд. который он назвал вытеенительным рядом металлов. Позднее (1802 г. В. Нерист) было доказано, что вытесни тельный ряд Векетовп практически совпадает с рядом, в котором металлы и водород расположены (направо) в порядке уменьшения их восствнояятеяьяой способности и молярной концентрации ионов металла, равна 1 моль/л. Этот ряд называют алектрохимычесиим рядам напряжений металлов. Вы уже знакомились с этим рядом, когда рассматривали взаимодействие кислот с металлами и выяснили, что с растворами кислот взаимодействуют металлы, которые расположены левее водорода. Это первое при вило ряда напряжений Оно выполняется с соблюдением ряда условий, о которых мы говорили ранее.
Второе правило ряда напряжений заключается в следующем: каждый металл вытесняет из растворов солей все другие металлы, расположенные правее его в ряду напряжений. Это правило также соблюдается при выполнении условий:
а) обе соли (и реагирующая, и образующяяся в результате реакции) должны быть растворимыми;
б) металлы ие должны аза имодействовать с водой , поэтому металлы главных подгрупп I и II групп (для последней начиная с Са) ие вытесняют другие металлы на растворов солей.
1. Соли средние (нормальные), кислые и основные.
2. Диссоциация различных груп солей.
3. Типичные свойства нормальных солей: взаимодействие их с кислотами, щелочами, другими солями и металлами.
4. Два правила ряда напряжений металлов.
5. Условия протекания реакций солей с металлами.
Закончите молекулярные уравнения возможных реакций, протекающих в растворах, и запишите соответствующие им ионные уравнения:

Если реакция не может быть осуществлена, объясните почему.
К 980 г 5% -го раствора сорной кислоты прилили избыток раствора нитрата бария. Найдите массу выпавшего осадка.
Запишите уравнения реакций всех возможных способов получения сульфата железа (II).
Дайте названия солей.
Притчи к уроку химии , картинки к уроку химии 8 класса , рефераты для школьников
Содержание урока конспект урока опорный каркас презентация урока акселеративные методы интерактивные технологии Практика задачи и упражнения самопроверка практикумы, тренинги, кейсы, квесты домашние задания дискуссионные вопросы риторические вопросы от учеников Иллюстрации аудио-, видеоклипы и мультимедиа фотографии, картинки графики, таблицы, схемы юмор, анекдоты, приколы, комиксы притчи, поговорки, кроссворды, цитаты Дополнения рефераты статьи фишки для любознательных шпаргалки учебники основные и дополнительные словарь терминов прочие Совершенствование учебников и уроков исправление ошибок в учебнике обновление фрагмента в учебнике элементы новаторства на уроке замена устаревших знаний новыми Только для учителей идеальные уроки календарный план на год методические рекомендации программы обсуждения Интегрированные урокиКак видно из определения, соли по составу похожи на кислоты, только вместо атомов водорода они содержат ионы металла. Поэтому их можно также назвать продуктами замещения атомов водорода в кислоте на ионы металла. Например, всем известная поваренная соль NaCl может быть рассмотрена как продукт замещения водорода в соляной кислоте НСl на ион натрия.
Заряд иона натрия 1+, а заряд иона хлора 1-. Так как соединение электронейтрально, формула поваренной соли Na + Cl - . Если же надо вывести формулу сульфида алюминия (III), поступают следующим образом.
- Обозначают заряды ионов, из которых состоит соединение: Al 3+ S 2- . Заряд иона алюминия 3+, а заряд иона серы можно определить по формуле соответствующей сероводородной кислоты H 2 S, он равен 2-.
- Находят наименьшее общее кратное числовых значений зарядов ионов алюминия и серы (3 и 2), оно равно 6.
- Находят индексы, разделив наименьшее общее кратное на величины зарядов, и записывают формулу:
Аналогично выводят формулы солей кислородсодержащих кислот, имеющих сложные ионы. Выведем, например, формулу кальциевой соли фосфорной кислоты - фосфата кальция. По таблице Менделеева определим заряд иона кальция как элемента главной подгруппы II группы (IIA группы): 2+. По формуле фосфорной кислоты Н 3 РO 4 определим заряд иона, образованного кислотным остатком: . Отсюда формула фосфата кальция имеет вид

(читают «кальций три, пэ-о-четыре дважды»).
Нетрудно заметить, что при выведении формул солей по зарядам ионов вы должны действовать так же, как при выведении формул бинарных соединений по валентности и по степеням окисления образующих их элементов.
Как образуют названия солей бескислородных кислот, вы уже рассмотрели, когда знакомились с номенклатурой бинарных соединений: соли НСl называют хлоридами, а соли H 2 S - сульфидами.
Названия солей кислородсодержащих кислот составляют из двух слов: названия иона, образованного кислотным остатком, в именительном падеже и названия иона металла - в родительном. Названия ионов кислотных остатков составляют, в свою очередь, из корней названий элементов, с суффиксами -am для высшей степени окисления и -ит для низшей степени окисления атомов элемента-неметалла, образующего сложный ион остатка кислородсодержащей кислоты. Например, соли азотной кислоты HNO 3 называют нитратами: KNO 3 - нитрат калия, а соли азотистой кислоты HNO 2 - нитритами: Ca(NO 2) 2 - нитрит кальция. Если же металл проявляет различные степени окисления, то их указывают в скобках римской цифрой, например: Fe 2+ SO 3 - сульфит железа (II) и - сульфат железа (III).
Номенклатура солей приведена в таблице 5.
Таблица 5
Номенклатура солей

По растворимости в воде соли делят на растворимые (Р), нерастворимые (Н) и малорастворимые (М). Для определения растворимости солей используют таблицу растворимости кислот, оснований и солей в воде. Если под рукой нет этой таблицы, можно воспользоваться приведёнными ниже правилами. Их легко запомнить.
- Растворимы все соли азотной кислоты - нитраты.
- Растворимы все соли соляной кислоты - хлориды, кроме AgCl (Н), РЬСl 2 (М).
- Растворимы все соли серной кислоты - сульфаты, кроме BaSO 4 (Н), PbSO 4 (Н), CaSO 4 (М), Ag 2 SO 4 (М).
- Растворимы соли натрия и калия.
- Не растворяются все фосфаты, карбонаты, силикаты и сульфиды, кроме этих солей для Na+ и К+.
Рассмотрим растворимую натриевую соль бескислородной соляной кислоты - хлорид натрия NaCl и нерастворимые кальциевые соли угольной и фосфорной кислот - карбонат кальция СаСO 3 и фосфат кальция Са 3 (РO 4) 2 .
Лабораторный опыт № 12
Ознакомление с коллекцией солей
-
Ознакомьтесь с коллекцией выданных вам образцов солей. Запишите их формулы, охарактеризуйте физические свойства, в том числе и растворимость в воде. Рассчитайте молекулярные (молярные) массы солей, а также массовые доли образующих их элементов. Найдите массу 2 моль каждой соли.
Хлорид натрия NaCl - хорошо растворимая в воде соль, известна под названием поваренная соль. Без этой соли невозможна жизнь растений, животных и человека, так как она обеспечивает важнейшие физиологические процессы в организмах: в крови соль создаёт необходимые условия для существования красных кровяных телец, в мышцах обусловливает способность к возбудимости, в желудке образует соляную кислоту, без которой было бы невозможным переваривание и усвоение пищи. Необходимость соли для жизни была известна со времён глубочайшей древности. Значение соли отражено в многочисленных пословицах, поговорках, обычаях. «Хлеб да соль» - вот одно из пожеланий, которым русские люди с давних пор обменивались друг с другом во время приёма пищи, подчёркивая равноценное с хлебом значение соли. Хлеб и соль стали символом гостеприимства и радушия русской нации.
Говорят: «Чтобы узнать человека, надо с ним пуд соли съесть». Оказывается, ждать не так уж долго: за два года двое съедают пуд соли (16 кг), так как в год каждый человек с пищей потребляет от 3 до 5,5 кг соли.
В названиях многих городов и посёлков разных стран присутствует слово соль: Соликамск, Соль-Илецк, Усолье, Усолье-Сибирское, Солт-Лейк-Сити, Солтвиль, Зальцбург и т. д.
Соль образует мощные отложения в земной коре. В Соль-Илецке, например, толщина пласта соли превышает полтора километра. Соли, находящейся в озере Баскунчак в Астраханской области, хватит нашей стране на 400 лет. Огромные количества соли содержат в себе воды морей и океанов. Солью, извлечённой из Мирового океана, можно было бы засыпать всю сушу земного шара слоем в 130 м. Во многих странах Азии и Африки соль добывают из соляных озёр (рис. 66, а), а в европейских странах - часто из соляных шахт (рис. 66, б).

Рис. 66.
Добыча соли:
а - из соляных озёр; б - из шахт
Хлорид натрия широко используют в химической промышленности для получения натрия, хлора, соляной кислоты, в медицине, для приготовления пищи, для консервирования продуктов питания (соление и квашение овощей) и т. д.
Карбонат кальция СаСO 3 - нерастворимая в воде соль, из которой многочисленные морские животные (моллюски, раки, простейшие) строят покровы своего тела - раковины (рис. 67) и кораллы.

Рис. 67.
Эти красивые раковины состоят преимущественно из карбоната кальция
Остатки коралловых полипов, с которыми вы познакомились на уроках биологии, образуют тропические острова (атоллы) и коралловые рифы (рис. 68). Наиболее известен Большой Барьерный риф в Австралии. Скапливаясь после гибели своих «хозяев» на дне водоёмов и главным образом морей, эти раковины за десятки и сотни миллионов лет сформировали мощные пласты соединений кальция, давших начало образованию горных пород - известняков СаСO 3 .

Рис. 68.
Красивейшие морские организмы - кораллы - строят свой скелет из карбоната кальция. Остатки их образуют коралловые атоллы и рифы
Эту же формулу имеет и строительный камень - мрамор, и столь привычный каждому стоящему у доски школьнику мел, который добывают из карьеров или меловых гор (рис. 69). Из известняка получают негашёную и гашёную известь, его применяют в строительстве. Мрамор идёт на изготовление статуй, им отделаны станции метро.

Рис. 69.
Меловые горы
Из карбоната кальция наземные животные «строят» свои скелеты - внутреннюю опору для мягких тканей, которые в десятки раз превышают вес самой опоры.
Фосфат кальция Са 3 (РO 4) 2 , нерастворимый в воде, - это основа минералов фосфоритов и апатитов. Из них производят фосфорные удобрения, без которых было бы невозможно получение высоких урожаев в сельском хозяйстве. Фосфат кальция также входит в состав костей животных.
Ключевые слова и словосочетания
- Соли.
- Номенклатура солей.
- Составление формул солей.
- Растворимые, нерастворимые и малорастворимые соли.
- Хлорид натрия (поваренная соль).
- Карбонат кальция (мел, мрамор, известняк).
- Фосфат кальция.
Работа с компьютером
- Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
- Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока - сделайте сообщение по ключевым словам и словосочетаниям следующего параграфа.
Вопросы и задания
- Составьте формулы солей натрия, кальция и алюминия для следующих кислот: азотной, серной и фосфорной. Дайте их названия. Какие из солей растворимы в воде?
- Запишите формулы следующих солей: а) карбоната калия, сульфида свинца (II), нитрата железа (III); б) хлорида свинца (IV), фосфата магния, нитрата алюминия.
- Из перечисленных формул: H 2 S, K 2 SO 3 , КОН, SO 3 , Fe(OH) 3 , FeO, N 2 O 3 , Cu 3 (PO 4) 2 , Cu 2 O, P 2 O 5 , H 3 PO 4 - выпишите формулы: а) оксидов; б) кислот; в) оснований; г) солей. Дайте названия веществ.
Химические свойства средних солей
Взаимодействие средних солей с металлами
Реакция соли с металлом протекает в том случае, если исходный свободный металл более активен, чем тот, который входит в состав исходной соли. Узнать о том, какой металл более активен, можно, воспользовавшись электрохимическим рядом напряжений металлов.
Так, например, железо взаимодействует с сульфатом меди в водном растворе, поскольку является более активным, чем медь (левее в ряду активности):
В то же время железо не реагирует с раствором хлорида цинка, поскольку оно менее активно, чем цинк:
Следует отметить, что такие активные металлы, как щелочные и щелочноземельные, при их добавлении к водным растворам солей будут прежде всего реагировать не с солью, а входящей в состав растворов водой.
Взаимодействие средних солей с гидроксидами металлов
Оговоримся, что под гидроксидами металлов в данном случае понимаются соединения вида Me(OH) x .
Для того чтобы средняя соль реагировала с гидроксидом металла, должны одновременно (!) выполняться два требования:
- в предполагаемых продуктах должен быть обнаружен осадок или газ;
- исходная соль и исходный гидроксид металла должны быть растворимы.
Рассмотрим пару случаев, для того чтобы усвоить данное правило.
Определим, какие из реакций ниже протекают, и напишем уравнения протекающих реакций:
- 1) PbS + KOH
- 2) FeCl 3 + NaOH
Рассмотрим первое взаимодействие сульфида свинца и гидроксида калия. Запишем предполагаемую реакцию ионного обмена и пометим ее слева и справа «шторками», обозначив таким образом, что пока не известно, протекает ли реакция на самом деле:
В предполагаемых продуктах мы видим гидроксид свинца (II), который, судя по таблице растворимости, нерастворим и должен выпадать в осадок. Однако, вывод о том, что реакция протекает, пока сделать нельзя, так как мы не проверили удовлетворение еще одного обязательного требования – растворимости исходных соли и гидроксида. Сульфид свинца – нерастворимая соль, а значит реакция не протекает, так как не выполняется одно из обязательных требований для протекания реакции между солью и гидроксидом металла. Т.е.:
Рассмотрим второе предполагаемое взаимодействие между хлоридом железа (III) и гидроксидом калия. Запишем предполагаемую реакцию ионного обмена и пометим ее слева и справа «шторками», как и в первом случае:
В предполагаемых продуктах мы видим гидроксид железа (III), который нерастворим и должен выпадать в осадок. Однако сделать вывод о протекании реакции пока еще нельзя. Для этого надо еще убедиться в растворимости исходных соли и гидроксида. Оба исходных вещества растворимы, значит мы можем сделать вывод о том, что реакция протекает. Запишем ее уравнение:
Реакции средних солей с кислотами
Средняя соль реагирует с кислотой в том случае, если образуется осадок или слабая кислота.
Распознать осадок среди предполагаемых продуктов практически всегда можно по таблице растворимости. Так, например, серная кислота реагирует с нитратом бария, поскольку в осадок выпадает нерастворимый сульфат бария:
Распознать слабую кислоту по таблице растворимости нельзя, поскольку многие слабые кислоты растворимы в воде. Поэтому список слабых кислот следует выучить. К слабым кислотам относят H 2 S, H 2 CO 3 , H 2 SO 3 , HF, HNO 2 , H 2 SiO 3 и все органические кислоты.
Так, например, соляная кислота реагирует с ацетатом натрия, поскольку образуется слабая органическая кислота (уксусная):
Следует отметить, что сероводород H 2 S является не только слабой кислотой, но и плохо растворим в воде, в связи с чем выделяется из нее в виде газа (с запахом тухлых яиц):
Кроме того, обязательно следует запомнить, что слабые кислоты — угольная и сернистая — являются неустойчивыми и практически сразу же после образования разлагаются на соответствующий кислотный оксид и воду:
Выше было сказано, что реакция соли с кислотой идет в том случае, если образуется осадок или слабая кислота. Т.е. если нет осадка и в предполагаемых продуктах присутствует сильная кислота, то реакция не пойдет. Однако есть случай, формально не попадающий под это правило, когда концентрированная серная кислота вытесняет хлороводород при действии на твердые хлориды:
Однако, если брать не концентрированную серную кислоту и твердый хлорид натрия, а растворы этих веществ, то реакция действительно не пойдет:
Реакции средних солей с другими средними солями
Реакция между средними солями протекает в том случае, если одновременно (!) выполняются два требования:
- исходные соли растворимы;
- в предполагаемых продуктах есть осадок или газ.
Например, сульфат бария не реагирует с карбонатом калия, поскольку несмотря на то что в предполагаемых продуктах есть осадок (карбонат бария), не выполняется требование растворимости исходных солей.
В то же время хлорид бария реагирует с карбонатом калия в растворе, поскольку обе исходные соли растворимы, а в продуктах есть осадок:
Газ при взаимодействии солей образуется в единственном случае – если смешивать при нагревании раствор любого нитрита с раствором любой соли аммония:
Причина образования газа (азота) заключается в том, что в растворе одновременно находятся катионы NH 4 + и анионы NO 2 — , образующие термически неустойчивый нитрит аммония, разлагающийся в соответствии с уравнением:
Реакции термического разложения солей
Разложение карбонатов
Все нерастворимые карбонаты, а также карбонаты лития и аммония термически неустойчивы и разлагаются при нагревании. Карбонаты металлов разлагаются до оксида металла и углекислого газа:
а карбонат аммония дает три продукта – аммиак, углекислый газ и воду:
Разложение нитратов
Абсолютно все нитраты разлагаются при нагревании, при этом тип разложения зависит от положения металла в ряду активности. Схема разложения нитратов металлов представлена на следующей иллюстрации:
Так, например, в соответствии с этой схемой уравнения разложения нитрата натрия, нитрата алюминия и нитрата ртути записываются следующим образом:
Также следует отметить специфику разложения нитрата аммония:
Разложение солей аммония
Термическое разложение солей аммония чаще всего сопровождается образованием аммиака:
В случае, если кислотный остаток обладает окислительными свойствами, вместо аммиака образуется какой-либо продукт его окисления, например, молекулярный азот N 2 или оксид азота (I):
Химические свойства кислых солей
Отношение кислых солей к щелочам и кислотам
Кислые соли реагируют с щелочами. При этом, если щелочь содержит тот же металл, что и кислая соль, то образуются средние соли:
Также, если в кислотном остатке кислой соли осталось два или более подвижных атомов водорода, как, например, в дигидрофосфате натрия, то возможно образование как средней:
так и другой кислой соли с меньшим числом атомов водорода в кислотном остатке:
Важно отметить, что кислые соли реагируют с любыми щелочами, в том числе и теми, которые образованы другим металлом. Например:
Кислые соли, образованные слабыми кислотами, реагируют с сильными кислотами аналогично соответствующим средним солям:
Термическое разложение кислых солей
Все кислые соли при нагревании разлагаются. В рамках программы ЕГЭ по химии из реакций разложения кислых солей следует усвоить, как разлагаются гидрокарбонаты. Гидрокарбонаты металлов разлагаются уже при температуре более 60 о С. При этом образуются карбонат металла, углекислый газ и вода:
Последние две реакции являются основной причиной образования накипи на поверхности водонагревательных элементов в электрических чайниках, стиральных машинах и т.д.
Гидрокарбонат аммония разлагается без твердого остатка с образованием двух газов и паров воды:
Химические свойства основных солей
Основные соли всегда реагируют со всеми сильными кислотами. При этом могут образоваться средние соли, если использовались кислота с тем же кислотным остатком, что и в основной соли, или смешанные соли, если кислотный остаток в основной соли отличается от кислотного остатка реагирующей с ней кислоты:
Также для основных солей характерны реакции разложения при нагревании, например:
Химические свойства комплексных солей (на примере соединений алюминия и цинка)
В рамках программы ЕГЭ по химии следует усвоить химические свойства таких комплексных соединений алюминия и цинка, как тетрагидроксоалюминаты и третрагидроксоцинкаты.
Тетрагидроксоалюминатами и тетрагидроксоцинкатами называют соли, анионы которых имеют формулы — и 2- соответственно. Рассмотрим химические свойства таких соединений на примере солей натрия:
Данные соединения, как и другие растворимые комплексные, хорошо диссоциируют, при этом практически все комплексные ионы (в квадратных скобках) остаются целыми и не диссоциируют дальше:
Действие избытка сильной кислоты на данные соединения приводит к образованию двух солей:
При действии же на них недостатка сильных кислот в новую соль переходит только активный металл. Алюминий и цинк в составе гидроксидов выпадают в осадок:
Осаждение гидроксидов алюминия и цинка сильными кислотами не является удачным выбором, поскольку сложно добавить строго необходимое для этого количество сильной кислоты, не растворив при этом часть осадка. По этой причине для этого используют углекислый газ, обладающий очень слабыми кислотными свойствами и благодаря этому не способный растворить осадок гидроксида:
В случае тетрагидроксоалюмината осаждение гидроксида также можно проводить, используя диоксид серы и сероводород:
В случае тетрагидроксоцинката осаждение сероводородом невозможно, поскольку в осадок вместо гидроксида цинка выпадает его сульфид:
При упаривании растворов тетрагидроксоцинката и тетрагидроксоалюмината с последующим прокаливанием данные соединения переходят соответственно в цинкат и алюминат.
В предыдущих разделах постоянно встречались реакции, в которых образуются соли.
Солями называются вещества, в которых атомы металла связаны с кислотными остатками.
Исключением являются соли аммония, в которых с кислотными остатками связаны не атомы металла, а частицы NH 4 + . Примеры типичных солей приведены ниже.
NaCl – хлорид натрия,
Na 2 SO 4 – сульфат натрия,
СаSO 4 – сульфат кальция,
СаCl 2 – хлорид кальция,
(NH 4) 2 SO 4 – сульфат аммония.
Формула соли строится с учетом валентностей металла и кислотного остатка. Практически все соли – ионные соединения, поэтому можно говорить, что в солях связаны между собой ионы металла и ионы кислотных остатков:
Na + Cl – – хлорид натрия
Ca 2+ SO 4 2– – сульфат кальция и т.д.
Названия солей составляются из названия кислотного остатка и названия металла. Главным в названии является кислотный остаток. Названия солей в зависимости от кислотного остатка показаны в таблице 4.6. В верхней части таблицы приведены кислородсодержащие кислотные остатки, в нижней – бескислородные.
Таблица 4-6. Построение названий солей.
|
Соль какой кислоты |
Кислот-ный остаток |
Валент-ность остатка |
Название солей | |
|
Азотная HNO 3 |
Ca(NO 3)2 нитрат кальция |
|||
|
Кремниевая H 2 SiO 3 |
силикаты |
Na 2 SiO 3 силикат натрия |
||
|
Серная H 2 SO 4 |
сульфаты |
PbSO 4 сульфат свинца |
||
|
Угольная H 2 CO 3 |
карбонаты |
Na 2 CO 3 карбонат натрия |
||
|
Фосфорная H 3 PO 4 |
AlPO 4 фосфат алюминия |
|
Бромоводородная HBr |
NaBr бромид натрия |
|||
|
Иодоводородная HI |
KI иодид калия |
|||
|
Сероводородная H 2 S |
сульфиды |
FeS сульфид железа (II) |
||
|
Соляная HCl |
NH 4 Cl хлорид аммония |
|||
|
Фтороводородная HF |
CaF 2 фторид кальция |
Из таблицы 4-6 видно, что названия кислородсодержащих солей имеют окончания «ат », а названия бескислородных солей – окончания «ид ».
В некоторых случаях для кислородсодержащих солей может использоваться окончание «ит ».Например, Na 2 SO 3 – сульфит натрия. Это делается для того, чтобы различать соли серной кислоты (H 2 SO 4) и сернистой кислоты (H 2 SO 3) и в других таких же случаях.
Все соли разделяются на средние, кислые и основные . Средние соли содержат только атомы металла и кислотного остатка. Например, все соли из таблицы 4-6 являются средними солями.
Любую соль можно получить соответствующей реакцией нейтрализации. Например, сульфит натрия образуется в реакции между сернистой кислотой и основанием (едким натром). При этом на 1 моль кислоты требуется взять 2 моля основания:
Если взять только 1 моль основания – то есть меньше, чем требуется для полной нейтрализации, то образуется кислая соль – гидросульфит натрия:
Кислые соли образуются многоосновными кислотами. Одноосновные кислоты кислых солей не образуют.
Кислые соли, помимо ионов металла и кислотного остатка, содержат ионы водорода.
Названия кислых солей содержат приставку «гидро» (от слова hydrogenium – водород). Например:
NaHCO 3 – гидрокарбонат натрия,
K 2 HPO 4 – гидрофосфат калия,
KH 2 PO 4 – дигидрофосфат калия.
Основные соли образуются при неполной нейтрализации основания. Названия основных солей образуют с помощью приставки «гидроксо». Ниже приведен пример, показывающий отличие основных солей от обычных (средних):
Основные соли, помимо ионов металла и кислотного остатка, содержат гидроксильные группы.
Основные соли образуются только из многокислотных оснований. Однокислотные основания таких солей образовать не могут.
В таблице 4.6 приведены международные названия солей. Однако полезно знать также русские названия и некоторые исторически сложившиеся, традиционные названия солей, имеющих важное значение (таблица 4.7).
Таблица 4.7. Международные, русские и традиционные названия некоторых важных солей.
|
Международное название |
Русское название |
Традиционное название |
Применение |
|
|
Карбонат натрия |
Натрий углекислый |
В быту – как моющее и чистящее средство |
||
|
Гидрокарбонат натрия |
Натрий углекислый кислый |
Питьевая сода |
Пищевой продукт: выпечка кондитерских изделий |
|
|
Карбонат калия |
Калий углекислый |
Применяется в технике |
||
|
Сульфат натрия |
Натрий сернокислый |
Глауберова соль |
Лекарственное средство |
|
|
Сульфат магния |
Магний сернокислый |
Английская соль |
Лекарственное средство |
|
|
Хлорат калия |
Калий хлорнова-токислый |
Бертолетова соль |
Применяется в зажигательных смесях для головок спичек |
Например, ни в коем случае нельзя путать соду Na 2 CO 3 и питьевую соду NaHCO 3 . Если нечаянно использовать в пищу соду вместо питьевой соды , можно получить тяжелый химический ожог.
В химии и в технике до сих пор сохраняется много старинных названий. Например, каустическая сода – вовсе не соль, а техническое название гидроксида натрия NaOH. Если обыкновенной содой можно почистить раковину или посуду, то каустическую соду ни при каких обстоятельствах брать в руки или использовать в быту нельзя!
Строение солей аналогично строению соответствующих кислот и оснований. Ниже приведены структурные формулы типичных средних, кислых и основных солей.

Приведем строение и название основной соли, формула которой выглядит: 2 CO 3 – дигидроксокарбонат железа (III). При рассмотрении структурной формулы такой соли становится ясно, что эта соль –продукт частичной нейтрализации гидроксида железа (III) угольной кислотой:

Соли - это продукты замещения водорода кислоты металлом или гидроксогрупп оснований кислотными остатками.
Например,
H 2 SO 4 + Zn = ZnSO 4 + Н 2
кислота соль
NaOH + НС1 = NaCl + H 2 O
основание кислота соль
С позиций теории электролитической диссоциации, соли – это электролиты, при диссоциации которых образуются катионы,отличные от катионов водорода, и анионы, отличные от анионов ОН - .
Классификация. Соли бывают средние, кислые, основные, двойные, комплексные.
Средняя соль - это продукт полного замещения водорода кислоты металлом или гидроксогруппы основания кислотным остатком. Например, Na 2 SO 4 , Ca(NO 3) 2 - средние соли.
Кислая соль - продукт неполного замещения водорода многоосновной кислоты металлом. Например, NaHSO 4 , Са(НСО 3) 2 - кислые соли.
Основная соль - продукт неполного замещения гидроксогрупп многокислотного основания кислотными остатками. Например, Mg(OН)С1, Bi(OH)Cl 2 - основные соли
Если атомы водорода в кислоте замещаются атомами разных металлов или гидроксогруппы оснований замещаются различными кислотными остатками, то образуются двойные соли. Например, KAl(SO 4) 2 , Са(ОС1)С1. Двойные соли существуют только в твердом состоянии.
Комплексные соли - это соли, в состав которых входят комплексные ионы. Например, соль K 4 - комплексная, так как в ее состав входит комплексный ион 4- .
Составление формул солей. Можно сказать, что соли состоят из остатков оснований и остатков кислот. При составлении формул солей нужно помнить правило: абсолютная величина произведения заряда остатка основания на число остатков основания равна абсолютной величине произведения заряда кислотного остатка на число кислотных остатков. Для тх = пу, где K - остаток основания, A - кислотный остаток, т - заряд остатка основания, n - заряд кислотного остатка, х - число остатков основания, у - число кислотных остатков. Например,
Номенклатура солей . Названия солей составляют из
названия аниона (кислотного остатка (табл.. 15)) в именительном падеже и названия катиона (остатка основания (табл. 17)) в родительном падеже (без слова «ион»).
Для названия катиона используют русское название соответствующего металла или группы атомов (в скобках римскими цифрами указывают степень окисления металла, если это необходимо).
Анионы бескислородных кислот называют, используя окончание –ид (NH 4 F – фторид аммония, SnS – сульфид олова (II), NaCN – цианид натрия). Окончания названий анионов кислородсодержащих кислот зависят от степени окисления кислотообразующего элемента:
Названия кислых и основных солей образуются по тем же общим правилам, что и названия средних солей. При этом название аниона кислой соли снабжают приставкой гидро- , указывающей на наличие незамещенных атомов водорода (число атомов водорода указывают греческими числительными приставками). Катион основной соли получает приставку гидроксо- , указывающую на наличие незамещенных гидроксогрупп.
Например,
MgС1 2 – хлорид магния
Ba 3 (РО 4) 2 – ортофосфат бария
Na 2 S – сульфид натрия
CaHPO 4 – гидрофосфат кальция
K 2 SO 3 – сульфит калия
Ca(H 2 PO 4) 2 – дигидрофосфат кальция
А1 2 (SO 4) 3 – сульфат алюминия
Mg(OH)Cl – хлорид гидроксомагния
КА1(SO 4) 2 – сульфат калия-алюминия
(MgOH) 2 SO 4 – сульфат гидроксомагния
KNaHPO 4 – гидрофосфат калия-натрия
MnCl 2 – хлорид марганца (II)
Са(OCI)C1 – хлорид-гипохлорит кальция
MnSO 4 – сульфат марганца (II)
К 2 S – cульфид калия
NaHCO 3 – гидрокарбонат натрия
К 2 SO 4 – сульфат калия